1. padoms. Kāpēc ūdens iztvaiko?
1. padoms. Kāpēc ūdens iztvaiko?
Iztvaicēšana ir dabisks fiziskais process, ko izraisa pastāvīga molekulu kustība šķidrumā. Ir svarīgi atzīmēt, ka ūdens iztvaikošana notiek jebkurā apkārtējās vides temperatūrā.
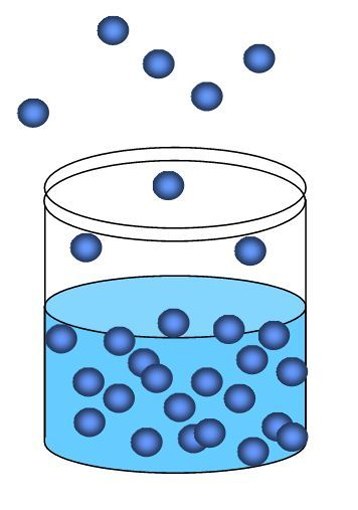
Ja konteiners ar ūdeni paliek atvērts, tad caurnoteiktā laika intervālā visu šķidrumu no tā iztvaiko. Iztvaikošana ir materiāla pārejas fiziskais process no šķidruma stāvokļa līdz gāzveida stāvoklim. Ūdenī, tāpat kā jebkurā citā šķidrumā, ir molekulas, kuru kinētiskā enerģija ļauj pārvarēt starpmolekulāro piesaisti. Šīs molekulas tiek paātrinātas un izkliedējas uz virsmas. Tāpēc, ja glāzi ūdens pārklāj ar papīra salveti, tad pēc brīža tas kļūs nedaudz mitrs. Bet ūdens iztvaikošana dažādos apstākļos notiek ar dažādām intensitātēm. Galvenie fiziskie raksturlielumi, kas ietekmē šī procesa plūsmas ātrumu un tā ilgumu, ir vielas blīvums, temperatūra, virsmas laukums, vēja klātbūtne. Jo lielāks ir vielas blīvums, jo tuvāk molekulas atrodas viens pret otru. Tātad, viņiem ir grūtāk pārvarēt starpmolekulāro piesaisti, un viņi lido daudz mazākā mērā ar virsmu. Ja divi šķidrumi ar dažādu blīvumu (piemēram, ūdeni un metilspirtu) tiek novietoti tādos pašos apstākļos, tad tas, kam ir mazāks blīvums, iztvaiko ātrāk. Ūdens blīvums ir 0,99 g / cm3, un metilspirta blīvums ir 0,79 g / cm3. Līdz ar to metanols iztvaiko ātrāk. Temperatūra ir arī svarīgs faktors, kas ietekmē ūdens iztvaikošanas ātrumu. Kā jau minēts, iztvaikošana notiek jebkurā temperatūrā, bet ar tās palielināšanos palielinās molekulu ātrums, un tie sāk šķidrumu atstāt lielākā daudzumā. Tāpēc dedzināšana ūdens iztvaiko ātrāk nekā auksts.Ūdens iztvaikošanas intensitāte ir atkarīga arī no tā virsmas laukuma. Ūdens, kas ielej pudelē ar šauru kaklu, iztvaiko lēnām, jo molekulas, kas izlido, apstāsies pudeles pudelēs, kas ir sašaurinājušās augšā un atgriežas atpakaļ. Ūdens molekula apakštase būs brīvi atstāt zhidkost.Protsess iztvaikošanu ievērojami paātrinātu ja virs virsmas, no kura iztvaikošanas notiek, tad gaisa plūsmas tiek pārvietots. Fakts ir tāds, ka papildus šķidruma molekulu atbrīvošanai notiek to atgriešanās. Un jo vairāk gaisa cirkulācijas, mazāk molekulas, kas iet uz leju, nonāks atpakaļ ūdenī. Tātad tā apjoms strauji samazināsies.
Padoms 2: kāpēc ūdens ir šķidrums
Dažādas ūdens īpašības daudzus gadusinterešu zinātnieki. Ūdens var būt dažādos stāvokļos - ciets, šķidrs un gāzveida. Parastā vidējā temperatūrā ūdens ir šķidruma formā. Jūs to varat dzert, ūdeni ar augiem. Ūdens var izplatīties un aizņemt noteiktas virsmas un izpausties kā tie kuģi, kuros tā atrodas. Tātad, kāpēc ir ūdens šķidrums?

Ūdens ir īpaša struktūra, kuras dēļnotiek kā šķidrums. Tas var ielej, plūst un pilināms. Cietvielu kristālos ir stingri noteikta kārtība. Gāzveida vielās struktūra tiek izteikta kā pilnīgs haoss. Ūdens ir starpnozaru struktūra starp cietu un gāzveida vielu. Daļiņas ūdens struktūrā atrodas nelielos attālumos viens no otra un ir salīdzinoši sakārtotas. Bet, tā kā daļiņas laika gaitā attālinās viens otru, arī struktūra struktūra ātri pazūd. Starpatomisko un starpmolekulāro mijiedarbību spēki nosaka vidējo attālumu starp daļiņām. Ūdens molekulas sastāv no skābekļa un ūdeņraža atomiem, pie kam skābekļa atomi vienā molekulā citas molekulas piesaistīto pret ūdeņraža atomiem. Veidojas unikālas ķēde ūdeņraža saites, kas dod ūdens atsevišķus plūsmas īpašības, struktūra ūdenī ir gandrīz identisks ar kristālisko struktūru. Ar daudzu eksperimentu palīdzību tika atklāts, ka pats ūdens pati veido brīvā tilpuma struktūru. Ja ūdens tiek apvienots ar cietām virsmām, ūdens struktūra sāk integrēties virsmas struktūrai. Tā kā ūdens robežslāņa struktūra nemainās, tās fizikāli ķīmiskās īpašības sāk mainīties. Ūdens viskozitāte mainās. Ir iespējams izšķīdināt vielas ar noteiktu struktūru un īpašībām. Ūdens sākotnēji ir dzidrs, bezkrāsains šķidrums. Ūdens fizikālās īpašības var saukt par anomālām, jo tai ir diezgan augsts viršanas punkts un sasalšanas temperatūra. Ūdens ir virsmas spraigums. Piemēram, tas ir anomāli augsta sasalšanas un vārīšanās temperatūra, kā arī virsmas spraigums. Īpaši iztvaikošanas un kušanas temperatūras robežas ūdens tuvumā ir daudz augstākas nekā jebkura cita viela. Apbrīnojama iezīme ir tā, ka ūdens blīvums ir lielāks par ledus blīvumu, kas ļauj ledus peldēt uz ūdens virsmas. Visas šīs brīnišķīgās ūdens īpašības, piemēram, šķidrumi, atkal ir izskaidrojamas ar to ūdeņraža saišu pastāvēšanu, ar kurām saistās molekulas. No ūdens molekulām trīs atomiem ģeometriskā projekcija tetraedra struktūra noved pie ļoti spēcīga savstarpēju piesaistei ūdens molekulām pret otru. Tas viss attiecas uz molekulu ūdeņraža saitēm, jo katra molekula var veidot četras pilnīgi identiskas ūdeņraža saites ar citām ūdens molekulām. Šis fakts arī izskaidro, ka ūdens ir šķidrs. Nav noslēpums, ka pasaulē ir mazāks saldūdens daudzums, un zinātnieki domā, kā atrisināt problēmu, iegūstot svaigu ūdeni ar ķīmiskām īpašībām. Ūdens šķidruma īpašības ļauj noskaidrot, kā ūdens ir iespējams mainīt un ietekmēt svaigu dzeramo ūdeni. Ūdens šķidrā stāvoklī var radīt enerģiju, piesātināt zemi, baro augus un organismus, ļaujot dzīvībai. Daudzi notikumi un laika apstākļi ir atkarīgi no ūdens un uzvedības uz zemes.







